Por Diana Bernal-Franco
Como
todos los seres vivos, los humanos estamos hechos en gran parte de proteínas,
las cuales determinan muchas de las características de nuestros cuerpos. Las proteínas
están codificadas por nuestro material genético, también conocido como ADN (Ácido DesoxirriboNucleico).
Por esta razón, las diferencias entre el ADN de diferentes individuos, son a la
larga las responsables por las diferencias entre individuos que hacen único a
cada ser humano. Desde el 2012 se ha venido consolidando una herramienta que permite
hacer cambios al ADN de forma muy precisa y relativamente fácil, conocida como CRISPR,
la cual está revolucionando la comunidad científica por las increíbles oportunidades
que abre para la investigación en medicina, agricultura y medio ambiente, y
esta generando grandes debates éticos por el potencial que tiene para
permitirnos crear bebes con características a nuestro antojo (Dance 2015).
¿Qué es CRISPR?
CRISPR es
una herramienta de ingeniería genética basada en un sistema de defensa que
tienen las bacterias. Cuando las bacterias son atacadas por virus, las
bacterias se defienden cortando el material genético de éstos, utilizando unas
“tijeras moleculares”, guiadas por ciertas secuencias que las bacterias han
guardado dentro su propio material genético de ataques anteriores. Dichas
secuencias tienen una estructura muy particular, que consta de una secuencia pequeña
de ADN, seguida por la misma secuencia pero en reversa (es decir secuencias
palindrómas), seguida por la secuencia que guía las “tijeras moleculares” hacia
el ADN viral, seguida por mas secuencias palindrómas. Toda esta estructura se
repite varias veces, cada vez secuencias que guía las “tijeras moleculares” hacia
diferentes ADN virales. De ahí su nombre CRISPR, que no es más que las siglas de
la descripción de la estructura de estas secuencias en inglés: Clustered Regularly Interspaced Short Palindromic Repeat. Desde
el 2012, unos cuatro grupos de investigación han venido desarrollado la tecnología
necesaria para convertir este sistema de defensa de las bacterias en una herramienta
que les permita a los científicos cortar secuencias específicas de ADN en
cualquier organismo (Pennisi 2013). Una vez los científicos cortan la secuencia
de ADN que desean, el sistema de reparación de ADN de cada organismo intenta
reparar el ADN cortado, pero este proceso es imperfecto, por lo cual la
secuencia de ADN queda, en efecto, modificada (Dance 2015), como se ilustra en
la figura 1.
Figura
1. Utilizando unas “tijeras moleculares” y una molécula guía de ARN -una molécula
fácil y barata de obtener- los científicos pueden hacer cambios a las
secuencias especificas de ADN que deseen. La molécula guía de ARN encuentra su
secuencia de ADN complementaria y la corta. Cuando el organismo intenta reparar
el corte ocurren errores y así la secuencia de ADN deseada queda modificada.
Basado en Pennisi 2013.
¿Cuáles son las ventajas de CRISPR?
Antes
de la aparición de CRISPR ya existían herramientas que permitían a los
científicos modificar el ADN. Sin embargo, dichas herramientas son muy
complejas y costosas, por lo que obtener resultados tangibles en un proyecto de
modificación del ADN tardaba meses. Ahora, con la llegada de CRISPR, se pueden
empezar a obtener resultados tangibles en cuestión de semanas (Pennisi 2013).
Esta gran ventaja de CRISPR se debe a que el reconocimiento del ADN a modificar
se logra a través de una molécula fácil de sintetizar y de almacenar, llamada
ARN (que es como una prima del ADN), mientras que en las herramientas
anteriores, el reconocimiento del ADN a modificar se basaba en proteínas, que
son moléculas difíciles de sintetizar y de almacenar. En consecuencia, los
experimentos basados en CRISPR son mucho más fáciles, baratos y rápidos de
realizar, por lo que CRISPR está reemplazando a las anteriores herramientas de modificación
del ADN en los laboratorios de investigación alrededor del mundo (Ledford
2015).
Aplicaciones de CRISPR y sus controversias
CRISPR
puede funcionar prácticamente en cualquier organismo. Se ha utilizado exitosamente
en levaduras, tabaco, arroz, ranas, ratones, conejos, y humanos (Sander and
Joung 2014). Así que CRISPR tiene el potencial de ser aplicado en campos tan variados
como el mejoramiento de plantas o animales, manejo ambiental y medicina.
Mejoramiento
de plantas o animales
CRISPR
representa una alternativa mucho menos costosa para modificar los genes de un
organismo, bien sea plantas o animales, que los métodos tradicionales de
transformación genética. En el caso de las plantas, se abre la posibilidad de
modificar genes de plantas de menor importancia económica que las que
tradicionalmente han sido mejoradas usando transformación genética, como el maíz
y la soya. Así, CRISPR ya se ha utilizado para producir naranjas enriquecidas
en vitaminas, y en el mejoramiento de animales, CRISPR se ha utilizado para
producir ganado sin cachos o cabras resistentes a ciertas enfermedades (Ledford
2015).
Por
otra parte, CRISPR genera grandes retos para la legislación que controla los
organismos genéticamente modificados −tema ya de por si muy espinoso (Palacios
2014)−. Tradicionalmente los organismos genéticamente modificados se definen
como organismos que poseen genes provenientes de otra especie de organismos. Por
lo tanto es fácil determinar si un organismo es genéticamente modificado si es
posible detectar el gen foráneo. En el caso de utilizar CRISPR para modificar
un organismo, aunque el organismo no tendría genes foráneos, si tendría genes
modificados con un objetivo especifico. Esto es diferente a que los organismos
que hayan sido sometidos a mutagénesis, los cuales si pueden ser comercializados
para consumo humano bajo la legislación actual. El utilizar CRISPR en el
mejoramiento de organismos implica que ya no sería fácil determinar si un
organismo es genéticamente modificado o si simplemente ha sido sometido a mutagénesis.
Por esto, al menos en los Estados Unidos, todavía no es claro cómo se regularan
los organismos generados con CRISPR (Ledford 2015).
Manejo
ambiental
En el
caso del manejo ambiental se ha propuesto introducir genes que disminuyan la
sobrevivencia de especies que tengan efectos negativos sobre los humanos, como
los mosquitos que transmiten la malaria o malezas que invaden los campos de
agricultura. Sin embargo las consecuencias de modificar genes en especies
silvestres podría tener consecuencias completamente impredecibles. Por ejemplo,
es posible que erradicar una especie invasiva en particular promueva la
aparición de otra especie invasiva, o que pasaría si se modifican genes
diferentes a los pretendidos? (Ledford 2015). Así que es muy importante evaluar
cuales podrían ser las consecuencias de utilizar CRISPR en especie silvestres,
sobretodo porque CRISPR permite crear un poderoso sistema de propagación de genes
modificados conocido como ‘gene drive’, el
cual hace que el gen modificado se salte las leyes normales de herencia e
invada una población natural muy rápidamente (Akbari et al. 2015), como se
ilustra en la figura 2.
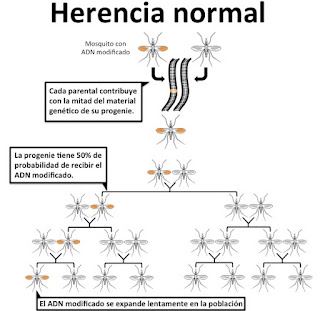
Figura
2. CRISPR se podría utilizar para propagar secuencias de ADN modificadas en
poblaciones naturales de manera muy rápida. Normalmente una secuencia
modificada se transmite solo a algunos individuos en cada generación, como se
ve la parte superior de la figura. CRISPR permitiría que un ADN modificado se
transmitiera a mas individuos de generación en generación, como se ve en la parte inferior, invadiendo poblaciones enteras en pocas generaciones. Basado en
Ledford 2015.
Una
aplicación de esta tecnología en el manejo ambiental, que está en las primeras
etapas de desarrollo, es generar un animal ecológicamente equivalente al mamut,
que se espera ayudaría a devolver la tundra a un ecosistema de pradera de
estepa. Antes, la tundra estaba cubierta de praderas que aislaban el permafrost
de la estepa, y los científicos han acumulado muchos datos que indican que el
mamut era una especie indispensable para el mantenimiento de dichas praderas.
Tras la extinción del mamut, las praderas desaparecieron, la estepa se
convirtió en tundra y el permafrost se está derritiendo. Si el permafrost de la
tundra se derritiera totalmente, liberaría 2.5 veces más gases de efecto
invernadero que si se quemaran todos los bosques del mundo, y los gases de
efecto invernadero son gran parte de la causa del calentamiento global (Lorena
2014). Por esto se busca obtener un animal equivalente al mamut que devuelva
las praderas a la tundra, y así proteger el permafrost de la tundra. La idea no
es revivir el mamut (lo cual es imposible porque los restos de mamut
encontrados tienen el ADN demasiado degradado), sino modificar los elefantes asiáticos
con adaptaciones que el mamut tenía, para crear un elefante modificado que
pudiera vivir en la estepa. En este sentido CRISPR ha sido fundamental en este
proyecto, ya que ha permitido a George Church y su equipo del instituto Wyss de
la Universidad de Harvard, introducir genes de mamut a células de elefante en
el laboratorio, a partir de las cuales potencialmente podrá surgir un elefante
modificado (visite http://longnow.org/revive/projects/woolly-mammoth/ para saber más de este
controversial proyecto).
En medicina
En el
caso de la medicina, CRISPR tiene muchísimas posibles aplicaciones. Por
ejemplo, es una herramienta prometedora para tratar pacientes afectados con el
virus del sida. Actualmente existen tratamientos que minimizan la actividad del
virus del sida, eliminado así los síntomas de la enfermedad prácticamente. Sin
embargo, el virus inserta su material genético dentro del ADN de algunas células
de los pacientes, y hasta ahora no hay tratamientos que puedan eliminar estas
inserciones, las cuales pueden re-activar el virus, sobre todo en pacientes de
mayor edad. Así que CRISPR ha sido utilizado exitosamente para eliminar el
material genético del virus en células humanas infectadas con el mismo, pero
hasta ahora estos experimentos solo se han llevado a cabo en el laboratorio (Hu
et al. 2014).
Además,
CRISPR también puede ser aplicado en combinación con otras tecnologías de
avanzada, abriendo la posibilidad de modificar el ADN de células germinales −es
decir espermatozoides u óvulos− y de embriones. Esta área de aplicación
requiere de un profundo análisis ético, particularmente al ser utilizada en
humanos, porque estas modificaciones genéticas podrían pasar a las siguientes
generaciones, lo cual conllevaría riesgos imposibles de prever. Además, se abre
la puerta a utilizar CRISPR para hacer cambios
genéticos no solo para curar enfermedades, sino para obtener características
deseables en un nuevo ser humano; una puerta que fácilmente nos puede llevar a prácticas
peligrosas y éticamente inaceptables (Cyranoski and Reardon 2015). El pasado
mes de Abril, un laboratorio de la Universidad de Guangzhou, de la China,
reportó la utilización de CRISPR para modificar genes en embriones humanos
(Liang et al. 2015). Aunque los embriones eran inviables, el estudio ha causado
un gran alboroto por ser el primer reporte de la aplicación de CRISPR en
embriones humanos; tanto, que aún antes de que el estudio fuera publicado,
varios de los científicos de Estados Unidos más influyentes en el área, como
Jennifer Doudna −una de las descubridoras de CRISPR− y George Church, hicieron
un llamado a poner un moratorio para que no se hagan modificaciones al ADN de
células germinales humanas en Nature
(Baltimore et al. 2015) y Science
(Lanphier et al. 2015), posiblemente la dos revistas científicas más
influyentes de nuestro tiempo. Sin embargo, investigadores del instituto
Francis Crick, el nuevo centro de investigación en biomédica de Londres,
pidieron autorización para editar genes en embriones utilizando CRISPR el
pasado 18 de Septiembre, con el objetivo de investigar el desarrollo
embrionario humano (Cressey et al. 2015).
Entre
tanto, mientras se dan los debates éticos, se establece el marco legal que
regirá el uso de CRISPR y se define quien se lleva el crédito intelectual, y de
paso, el control de las patentes sobre CRISPR −las que están siendo disputadas
por Jennifer Doudna y Feng Zhang, investigador del Instituto de Tecnología de
Massachusetts y de la Universidad de Harvard (Regalado 2015)− muchos
laboratorios alrededor del mundo continúan optimizando la tecnología CRISPR y utilizándola
en los proyectos más significativos e impactantes del momento.
Referencias
Akbari,
O. S., Hugo J Bellen, Ethan Bier, Simon L Bullock, Austin Burt, George M
Church, Kevin R Cook, et al. 2015. “Safeguarding Gene Drive Experiments in the
Laboratory.” Science 349 (6251) (August 28): 927–929.
Baltimore,
D., Paul Berg, Michael Botchan, Dana Carroll, R Alta Charo, George Church,
Jacob E Corn, et al. 2015. “A Prudent Path Forward for Genomic Engineering and
Germline Gene Modification.” Science 348 (6230) (April 3): 36–38.
Cyranoski,
David, and Sara Reardon. 2015. “Embryo Editing Sparks Epic Debate.” Nature 520
(7549) (April 29): 593–595.
Cressey,
D., Abbott, A. and Ledford, H. 2015. “UK scientists apply for licence to edit
genes in human embryos”. Nature Publishing Group. Tomado de
http://www.nature.com/news/uk-scientists-apply-for-licence-to-edit-genes-in-human-embryos-1.18394
en Septiembre de 2015.
Dance,
Amber. 2015. “Core Concept: CRISPR Gene Editing.” Proceedings of the National
Academy of Sciences 112 (20): 6245–6246.
Hu,
Wenhui, Rafal Kaminski, Fan Yang, Yonggang Zhang, Laura Cosentino, Fang Li,
Biao Luo, et al. 2014. “RNA-Directed Gene Editing Specifically Eradicates
Latent and Prevents New HIV-1 Infection.” Proceedings of the National Academy
of Sciences of the United States of America 111 (31): 11461–11466.
Lanphier,
Edward, Fyodor Urnov, Sarah Ehlen Haecker, Michael Werner, and Joanna
Smolenski. 2015. “Don’t Edit the Human Germ Line.” Nature 519 (7544) (March
12): 410–411.
Ledford,
Heidi. 2015. “CRISPR, the Disruptor.” Nature 522 (7554) (June 3): 20–24.
Liang,
Puping, Yanwen Xu, Xiya Zhang, Chenhui Ding, Rui Huang, Zhen Zhang, Jie Lv, et
al. 2015. “CRISPR/Cas9-Mediated Gene Editing in Human Tripronuclear Zygotes.”
Protein & Cell 6 (5): 363–372.
Palacios,
Juan Diego. 2014. “Reconsiderando la critica a los Organismos Genéticamente
Modificados”. http://biogenic-colombia.blogspot.com/2014_04_01_archive.html
Pennisi,
Elizabeth. 2013. “The CRISPR Craze.” Science 341 (6148): 833–836.
López-Galvis,
Lorena. 2014. “Cambio climático: ¿es verdad que hay un cambio?”.
http://biogenic-colombia.blogspot.com/2014/10/cambio-climatico-es-verdad-que-hay-un.html.
Regalado,
Antonio. 2015. “El hallazgo biotecnológico del siglo está envuelto en una
guerra de patentes”. MIT Technology review. Traducido por Lia Moya. Tomado de
http://www.technologyreview.es/biomedicina/46583/el-hallazgo-biotecnologico-del-siglo-esta/
en Septiembre de 2015.
Sander,
Jeffry D, and J Keith Joung. 2014. “CRISPR-Cas Systems for Editing, Regulating
and Targeting Genomes.” Nature Biotechnology 32 (4): 347–55.








0 comments to “CRISPR, una herramienta para editar el genoma que está revolucionando la ciencia”